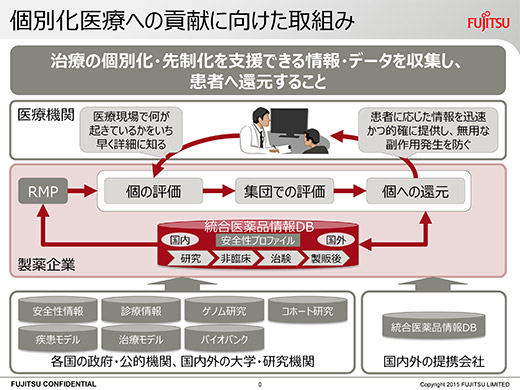
患者データを一つに集約‐“患者個々の医療”へ照準
富士通は、個別化医療や先制医療を支援できるデータを収集し、患者へと還元するファーマコビジランス活動のあるべき姿に向け、安全性管理業務の新たなソリューションの構築に取り組んでいる。それを実現するための情報基盤が、探索から非臨床、治験、製造販売後までの医薬品開発に関するデータを統合し、部門横断的な情報共有を目指した「統合医薬品情報データベース」だ。創薬から育薬までライフサイクル全般で収集したデータから、導き出された安全性プロファイルと、その根拠となるデータ群を関連づけて蓄積し、医薬品開発に携わる関係者が個々の患者に応じて、新しい事実や情報を抽出・活用できるためのICTソリューションを提供するという取り組みに着手した。ビッグデータを活用し、個別化医療に根ざした医薬品開発に対応していくことで、製薬企業の医薬品リスク管理計画(RMP)の有用性を発揮していく考えだ。
同社は、製薬企業に対して、探索段階での「IT創薬」から、非臨床・臨床におけるデータ収集・評価、さらに製販後領域と事業活動の全般にわたって、ソリューションを提供している。医療機関に対しても、電子カルテなどの提供を通じて緊密なネットワークを持っており、「製薬企業」と「病院」、「基礎」と「臨床」を橋渡しできる数少ないICTベンダーといえる。
RMPの作成から運用をサポートするのは、製薬企業向けに医薬品の開発から製販後までの安全性管理業務を支援するクラウドサービス「tsClinical」(ティーエスクリニカル)が柱。
特に製販後領域では、関連会社の「富士通エフ・アイ・ピー」が製造販売後調査(PMS)データ収集システム「PostMaNet」(ポストマネット)や、安全性情報管理ソリューション「パーシヴAce/PV」(パーシヴエースピーヴイ)などを提供し、国内で高いシェアを獲得している。
ただ、RMPを取り巻く環境は課題が山積している。医薬品の安全性、有効性、有用性に関する情報については、非臨床・治験・製造販売後の領域ごとに分散しているのが実態で、十分に活用・応用できているとはいえない。特に医薬品の安全対策においては、強化された規制へ対応していくことに手一杯で、患者個々に有用な情報を収集・提供する余裕がないとの課題に直面している。
「部門間連携」と「データの利活用」という製薬企業が抱える二つの課題に対し、富士通が提案するのが、部門横断的な情報共有を可能にした「統合医薬品情報データベース」と、膨大な医薬品情報の中から、患者の遺伝的背景・疾患の状態を考慮して新たな事実・情報を引き出す「データマイニング」の解決策だ。
統合医薬品情報データベースでは、多種多様な情報を統合・解析するために、CDISC標準に基づく「メタデータレポジトリ」の構築に取り組んでいる。医薬品医療機器総合機構が2016年にCDISC標準での承認申請の受付を開始する中、同社はメタデータレポジトリを通じて、承認申請にとどまらず、安全性業務の改善から、米FDAが推奨する治験開始のIND申請を目的としたSENDデータセット対応や、薬剤の薬理作用から別適応症を探る「ドラッグリポジショニング」、実臨床での観察研究など様々な用途での活用を目指す。
探索研究から製造販売後まで医薬品に関する情報を統合し、長期間にわたって保存でき、膨大な医薬品情報から自動的に新しい事実・情報を抽出することを可能にする、同社の新安全性管理業務ソリューション。規制当局からの高い要求事項に応えると共に、共同開発先やライセンス先、CROとの情報交換を円滑にし、医師や薬剤師、患者との関係性向上につなげ、目指す高みは大規模な医療データを活用した個別化医療だ。まずはRMPで成功させ、製薬企業への適用とアカデミア・医療機関との連携を通じて、医薬品の価値最大化を実現させる。
富士通株式会社
http://www.fujitsu.com/jp/solutions/industry/life-sciences/