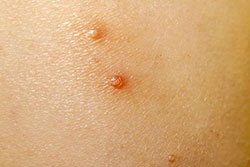
Photo Credit: Adobe Stock
米食品医薬品局(FDA)は7月24日、成人および2歳以上の小児における伝染性軟属腫(水いぼ)の局所治療薬としてYcanth(一般名カンタリジン)を承認した。水いぼ治療薬のFDAによる承認は今回が初めて。
Ycanthは、医薬品の製造管理および品質管理の基準(Good Manufacturing Practice;GMP)で管理されたカンタリジン(0.7%)製剤を1回使い切りのアプリケーターにより局所に塗布するもの。GMPとは、原材料の調達から製造、出荷に至るまでの全過程において、製品の「安全性」と「一定の品質」を保つために定められた規則とシステムのこと。投与は医療従事者が行い、投与頻度は3週間ごとに1回である。
今回の承認は、2〜60歳の水いぼ患者を対象にした2件の第3相試験(CAMP-1とCAMP-2、試験参加者の総計は528人)の結果に基づいている。主要評価項目とされた、治療を受けた水いぼの84日目までの完全消失を達成した対象者の割合は、年齢に関わりなく、Ycanth群の方がプラセボ群よりも統計学的に有意に高かった。具体的には、完全消失を達成した対象者の割合は、CAMP-1ではYcanth群46%、プラセボ群18%、CAMP-2では同順で54%と13%であった(いずれもP<0.0001)。
Ycanthによる治療で最もよく生じた有害反応は、塗布部位の皮膚反応(水疱、疼痛、かゆみ、かさぶた、発赤、変色、乾燥、浮腫、皮膚のびらん)で、Ycanthを投与したほとんどの対象者(97%)に発現した。重篤な副作用は報告されなかった。有害反応による治療中断率はYcanth群で2.3%、プラセボ群で0.5%だった。
Ycanthの承認はVerrica Pharmaceuticals社に対して与えられた。同社の社長兼最高経営責任者(CEO)であるTed White氏は、「この承認は、皮膚科医療における歴史的な転換点となるものだ。医師、患者、介護者は、長きにわたり、安全で効果的なFDA承認の水いぼ治療薬を求めてきた。水いぼは、皮膚と皮膚の接触や、ウイルス性病変で汚染された物の共有を通じて広がるため、局所に確実に塗布できる治療薬が感染拡大を阻止する上では不可欠だ」と同社のニュースリリースで語っている。同氏はまた、「Verrica社が実施した臨床試験の結果に基づき、Ycanthが2歳の患者にも安全かつ有効であることがFDAにより認められ、水いぼと闘う患者と医療従事者にとって重要な治療選択肢がもたらされることになった」と述べている。(HealthDay News 2023年7月24日)
Source
https://consumer.healthday.com/molluscum-2662328057.html
More Information
https://www.fda.gov/drugs/news-events-human-drugs/fda-approves-first-treatment-molluscum-contagiosum




















