Photo Credit: Adobe Stock
米食品医薬品局(FDA)は、7月23日、成人の慢性手湿疹(CHE)の治療薬として、LEO Pharma社の外用薬Anzupgo(一般名デルゴシチニブ)クリームを承認した。CHEに特化した治療薬が米国で承認されるのは今回が初めて。対象は、局所ステロイドが推奨されない、または局所ステロイドが十分な効果を発揮しない中等症から重症のCHE成人患者である。Anzupgoは、ヤヌスキナーゼ(JAK)阻害薬で、手湿疹の炎症に関与するJAK-STAT経路を抑制して炎症性サイトカインの活性化を防ぎ、皮膚の炎症反応を緩和する。
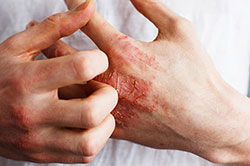
全米湿疹協会によると、CHEは、手や手首に赤み、痒み、ひび割れなどの症状が3カ月以上続くか、年に2回以上再発する手湿疹と定義される。世界人口のおよそ10人に1人がCHEに罹患しているとされる。手湿疹の発症には、遺伝的要因や刺激物、アレルゲンへの曝露が関与しており、特に、清掃業、美容業、医療従事者など、化学物質と接触する可能性の高い職業に従事する人でリスクが高い。過去の研究では、CHEは患者の生活の質(QOL)やメンタルヘルスに深刻な悪影響を及ぼす可能性が示唆されている。
Anzupgoの有効性は、ステロイド外用薬の効果が不十分か、または使用が推奨されなかった中等症から重症のCHEを有する18歳以上の患者(計960人)を対象にした2件のランダム化⼆重盲検対照試験(試験1、2)で評価された。対象者は16週間にわたり、⼿と⼿⾸の患部に1⽇2回、局所⽤Anzupgoまたはプラセボのいずれかを塗布した。
その結果、16週⽬にInvestigator Global Assessment of Chronic Hand Eczema(IGA-CHE)による手湿疹の重症度評価で治療成功を達成した者の割合は、試験1ではプラセボ群10%だったのに対しAnzupgo群は20%、試験2ではプラセボ群7%に対し、Anzupgo群は29%と、両試験ともにAnzupgo群の方が有意に改善したことが示された。
全米湿疹協会のCEO兼会長であるKristin Belleson氏は、「FDAが中等症から重症のCHEが患者に与える影響を認識していることに感激している。CHEのような日常生活機能を低下させる疾患と付き合うことは非常に困難であり、仕事や、人との触れ合いや物に触れること、大切な人々とのつながりに影響を及ぼしかねない。今回の承認は、CHE患者とその関係者や、さらに、その不快な症状からの永続的な解放を求める人々に希望と可能性を与えるものである」とLEO Pharma社のリリースで述べた。
なお、Anzupgoは、すでにEU(欧州連合)、英国、スイス、アラブ首長国連邦で承認されている。(HealthDay News 2025年7月24日)
Source
https://www.healthday.com/health-news/fda-approves-first-cream-for-treating-chronic-hand-eczema
More Information
https://www.leo-pharma.us/AnzupgoPI
https://www.leo-pharma.com/media-center/news/2025-fda-approval
https://nationaleczema.org/types-of-eczema/hand-eczema/