北海道大学大学院薬学研究院・卓越教授 原島 秀吉

2010年当時のDDS領域では、リポソーム、高分子ミセル、デンドリマー、ナノゲルなど種々のDDSがその性能を競っていたが、10年に衝撃的な論文が現れた。DLin-KC2-DMAというionizable cationic lipid(iCL)がsiRNAの肝臓送達において、ED50=0.02mg/kgという桁違いのサイレンシング効果の誘導に成功した(Nat. Biotech. 28:172-176,2010)
iCLのコンセプトは、カナダ・ブリティッシュコロンビア大学のPieter Cullis教授の発案で、テクミラ社、アルナイラム社との共同で完成させたブレークスルーテクノロジーである。当時、われわれの研究室で最も高効率であったR8/GALA-MENDの活性はED50=1~2mg/kgで、約100倍の違いが見られ、われわれの検討では100倍も改善できる伸びしろはなかった。
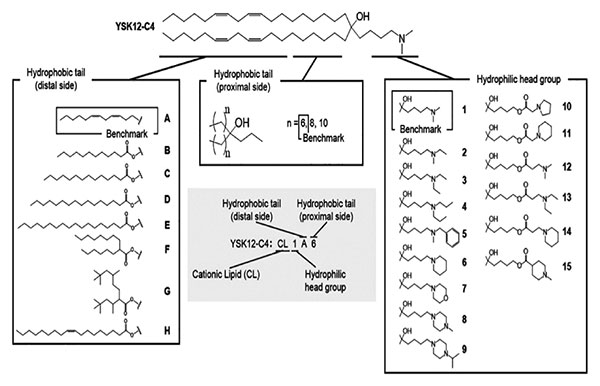
当時、大学院生の佐藤悠介君が未来創剤学研究室でアプタマーリガンドの合成を行っていた兵藤守特任助教から有機合成の指導を受けて、iCLのコンセプトに基づいて独自の構造を持つiCLを設計し、YSK05と命名した。その結果、ED50=0.06mg/kgという高活性が得られ、iCLの卓越性が明確になった。
そこで、iCLへ方針変更を決断し、さらなる改良を行いYSK12、YSK13などを設計・評価したところ、YSK13は肝臓におけるサイレンシング効果においてED50=0.01mg/kgで、DLin-KC2-DMAと同等以上の活性を示した。
Cullis教授、テクミラ社、アルナイラム社は、DLin-KC2-DMAをベンチマークとしてさらなる脂質ライブラリーを構築し、数百という誘導体の中からin vivoスクリーニングによりDLin-MC3-DMA(以下MC3)という超高活性のiCLの探索に成功し(ED50=0.005mg/kg)、18年には世界初のsiRNAナノ医薬品「オンパットロ」が誕生した。
MC3は、核酸ナノ医療の幕を開くと同時に、iCLのゴールドスタンダードになった。われわれは、in vitroでサイレンシング活性が高く、かつ物質特許の取得にも成功したYSK12-C4をベンチマークとして、親水性頭部と疎水性脂質足場の両方の構造を変化させることで、より広い構造スペースを検討した結果、CL4H6(ED50=0.0025mg/kg)というMC3を超えるiCLの探索に成功した(PCT/JP2018/022940)
CL4H6は、われわれの従来型の400倍のサイレンシング活性を実現し、MC3を凌駕した。
20年にパンデミックとなったCOVID-19に対するmRNAワクチンが、ファイザー・ビオンテック社により1年以内という驚異的なスピードで開発され、アストラゼネカ・オックスフォード大学のアデノウイルスベクターを用いたワクチンよりも優れたワクチン効果を誘導することに成功したのも、MC3をさらに改良したALC-0315というiCLの貢献が大きい。
現在、これらの新規iCLは、mRNA送達やゲノム編集の応用へと展開している。
本研究が大学発革新的医薬品の創出に寄与することを願い、北海道大学産学連携本部の全面的な協力のもと、CL4H6を含むiCLライブラリーの特許出願を行い、北大独自のビジネスモデルに基づいて多数の企業(海外メガファーマ、ベンチャー企業)と大型共同研究、オプション契約やライセンス契約を提携し、社会実装を進めている。