慶應義塾大学 医学部 教授 谷川原 祐介

「薬物治療はなぜ、全員に効かないのか」「薬理反応の個人差はなぜ、生じるのか」「科学的かつ合理的に用法用量を最適化するにはどうすれば良いのか」。これが私の研究の原点となったリサーチ・クエスチョンである。
40年間一貫して、薬学を基盤として臨床医学との融合領域を切り拓き、よって薬物療法の科学性の向上をめざす研究をライフワークとして続けてきた。振り返れば、3大学での病院薬剤部および医学部臨床系教室に職を得て、常に医学・医療を眼前に意識しつつ、薬学サイエンスを考えるという自身が置かれてきた環境が大きく影響していると思う。
これらのリサーチ・クエスチョンに対して、私は臨床医学領域に薬物体内動態(PK)、薬物曝露と効果・副作用の関係(PD)、ファーマコゲノミクス(PGx)などの薬学サイエンスを導入して、薬学と臨床医学の融合領域を切り拓き、薬物治療の最適化をめざす研究とその実践に力を尽くしてきた。
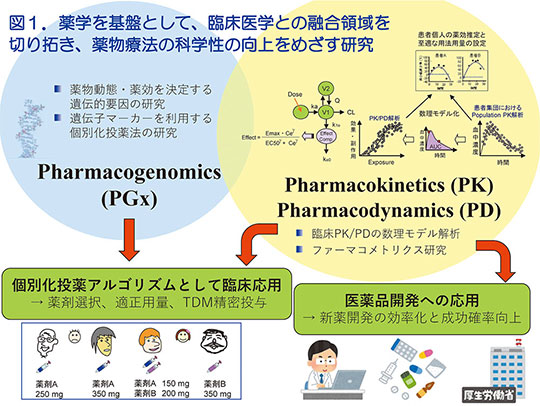
医療現場においては、薬物体内動態の個人差や遺伝的多様性を研究し、TDMをはじめとする個別化投薬手法の臨床応用に努めた。同時に、PK/PD研究手法を医薬品開発にも応用し、新薬の至適用量を科学的かつ効率的に見出すなど創薬領域への応用を先導してきた(図1)
薬物治療の最適化は、[1]投与量の最適化と[2]薬剤選択の最適化――の両方を満たすことにより達成される。投与量は、用量―薬物体内動態―治療効果の3者の関係と各患者の病態生理を加味した定量的考察によって最適化する必要があり、一方で適切な薬剤は各患者の薬剤反応性に基づいて選択されるべきである。私は、[1]の定量的考察を数理モデルとシミュレーションを駆使する臨床PK/PD研究によって深め、[2]についてはPGxに着目した。
薬学サイエンスの実地医療への実装においては、治療効果の個人差が大きい抗てんかん薬、ジゴキシン、抗菌薬、免疫抑制薬などについて、TDMと母集団薬物動態解析を組み合わせることにより精度良く個人の至適投与量を設定できる治療アルゴリズムを研究し、普及に努めた。
1980年代の薬剤師の臨床業務黎明期には、これらは薬剤師の病棟活動を支える重要な学術的基盤となった。
一方で、医薬品開発研究への展開においては、効率的かつ合理的に適正用量を設定する手法の研究と共に、治験から除外される特別な背景を有する患者(臓器機能低下、併存疾患、高齢者等)に対する適正用量を見出すために、PK/PD研究を推進し、抗菌薬、抗癌薬、降圧薬、骨粗鬆症薬など様々な疾患領域における治療薬開発に貢献することができた。
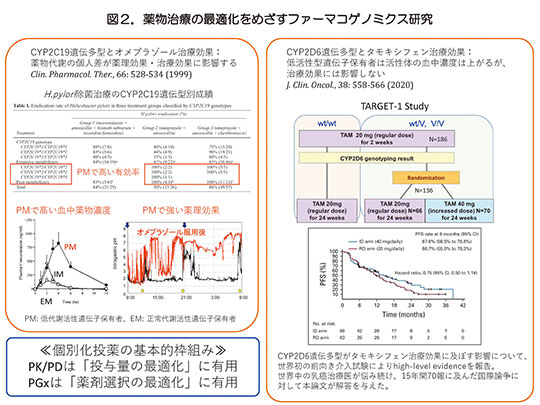
さらに、ヒトゲノムの多様性に基づき、薬剤反応性と遺伝多型の関連性に着目した研究を進めてきた。薬物代謝酵素CYP2C19遺伝多型が薬理効果に影響し、治療効果にも影響するオメプラゾールのケースもあれば、CYP2D6遺伝多型はタモキシフェン代謝には影響するが治療効果とは関連しないという知見も見出し、全容解明にはPK/PD/PGxが絡み合った複雑系を丁寧に解きほぐす必要があることを示した(図2)。複雑系の解析には実証科学手法に加えて、データ・サイエンスの力が必須となる。
冒頭に述べた研究を開始して40年が経過した今、個別化医療は世界の潮流となり、最適な薬剤は各個人の病態生理や遺伝的背景に基づいて選択され、最適な用量は各個人のPK/PDに基づいて決定されるというのが到達した結論である。
私が臨床医学と薬学の境界領域に身を置いて歩んだ40年は、薬学や薬剤師がモノ(製薬)から人(臨床)へ拡張、転換した歴史と重なる。そして、これからの薬学はそれらに加えてデータ・サイエンスを新たなツールとして活用し、生命現象の研究や疾病の治療開発研究における複雑系の解明に取り組む必要があるだろう。