東京大学大学院薬学系研究科教授 大和田 智彦

私たちの研究グループは新しい化学現象、特に窒素原子を含む化学結合の活性化に興味を持ち、新たな性質を持つ化学結合を発見してきた。この純粋な有機化学の発見が、思いがけず機能のある物質、特に生物活性のある分子の創製につながった。薬学研究の一つの典型を示せたのではないかと自負している。以下の四つの研究内容を概説する。
◇ ◇
非平面アミドに基づく規則構造の創出と天然アミノ酸規則構造との相互作用
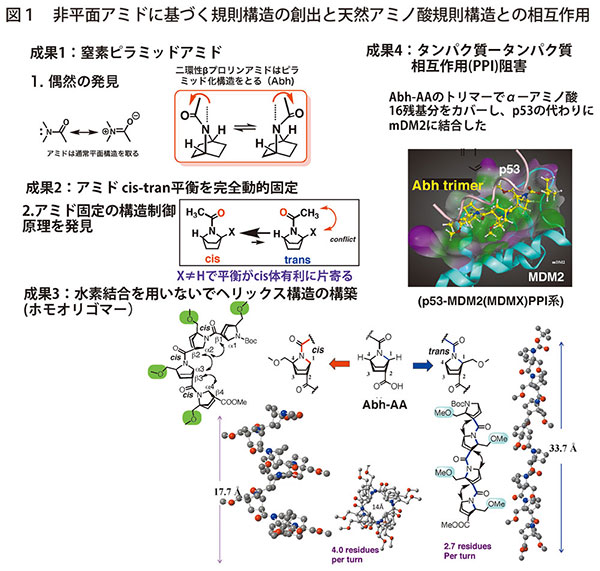
アミドのC-N結合は二重結合性を持ち平面構造を取る。もしアミド窒素が平面ではなくピラミッド化すると、共鳴安定化が得られず不安定化し、水で速やかに加水分解される。偶然にも、二環性構造(7-アザビシクロ[2.2.2]ヘプタン)に組み込まれた窒素原子が作る安定な窒素ピラミッドアミドを発見した(図1:成果1)。二環性構造にカルボン酸をβ-アミノ酸を作るように導入し、アミド結合をペプチド(Abh-AA)として利用し、ホモオリゴマーを合成すると水素結合によらないヘリックス構造を創出した(図1:成果3)。この規則構造の堅牢性を実現するためにはアミドのシス・トランス平衡の完全制御が必要だった(図1:成果2)。この天然に存在しない規則性を持つヘリックス分子は、タンパク質-タンパク質相互作用を阻害した(図1:成果4)
◇ ◇
N-NO結合の開裂制御
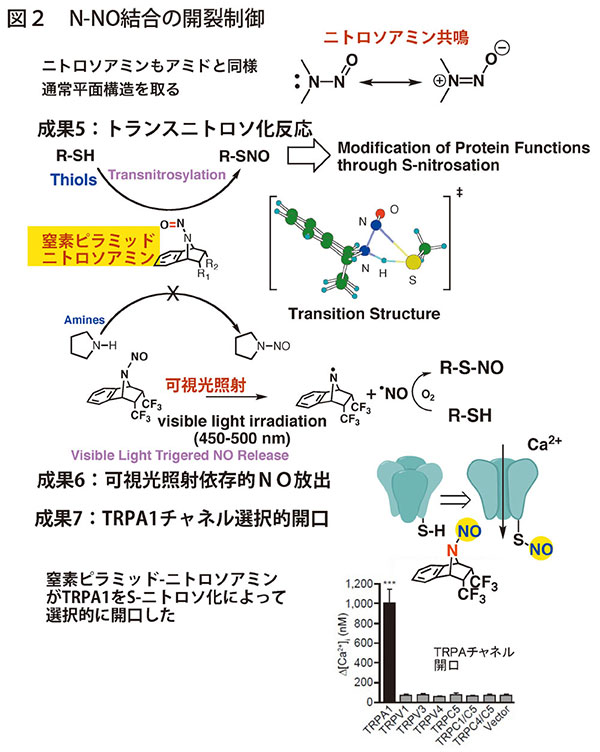
アミドと同様にN-ニトロソアミンにおいても、窒素がピラミッド化し、二重結合性の減弱したN-NO結合がシステインなどのチオールと反応して、S-ニトロソ化反応を起こした(図2:成果5)。S-ニトロソ化を介してTRPAチャネルの選択的開口作用を発揮した(図2:成果7)。さらに、窒素ピラミッド化によりニトロソアミンの吸収が長波長シフトし、可視光照射によるNO放出能も明らかにした(図2:成果6)。なお、これらのN-ニトロソアミンは二環性構造ゆえに変異原性を持たない。
◇ ◇
窒素カチオンへの隣接基関与による新カチオン化学反応の発見
隣接基関与は炭素カチオンについて研究されているが、他のカチオンでの関与は未解明のままだった。
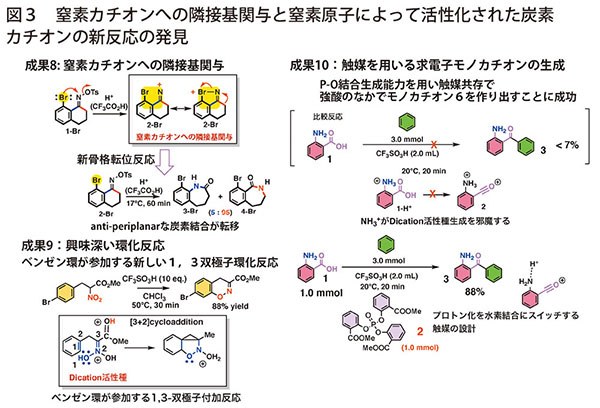
オキシムから生成するsp2型窒素カチオンが隣接するヘテロ原子と一過的に結合を形成し、新たな転位反応を引き起こした(図3:成果8)
◇ ◇
窒素原子によって活性化された炭素カチオンの新反応の発見
酸存在下、ニトロ基の酸素原子がベンゼン環上に環化する反応を見出した。単純な求電子置換ではなく、芳香環を含む1,3双極子環化付加反応であることを突き止めた(図3:成果9)。またアミンとカルボン酸が共存する分子では、酸存在下アミンのプロトン化がカルボン酸のイオン化を阻害する。アミンのプロトンを引き離し水素結合に変換することで、芳香族アシル化を促進するリン酸エステル触媒を見出した(図3:成果10)
直感的なテーマ展開にも関わらず自分を信じて一緒に研究を行っていただいた学生の皆様に感謝申し上げます。