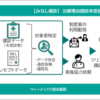
大手ジェネリック医薬品メーカーの大洋薬品工業が、承認規格外製品を出荷・流通させたことに対し、岐阜県健康福祉部薬務水道課は、薬事法第56条に対する違反として業務停止命令を出すことを決めた。業務停止期間は今月下旬から10日間前後の見込み。製造ミスがあったのは、高山工場(岐阜県高山市)で製造された抗潰瘍剤「ガスポートD錠20mg」(一般名:ファモチジン)で、既に昨年9月に自主回収されている。
大洋薬品によると、問題となったのは「ガスポートD錠20mg」の2ロットで、昨年2月に製造し、4~9月に出荷した約2万8500箱(1箱100錠)。主成分のファモチジン配合量が、厚生労働省への申請規格から外れていた。同社は主成分の配合量を1錠当たり20mgと定め、誤差範囲を5%以内としていたが、1ロットでは20%多く、もう1ロットでは20%少なかった。昨年9月28日から自主回収を開始した際には、「製造工程における不具合と、出荷試験用サンプリングのミスに由来」することを原因に挙げている。
配合量ミスが分かったのは、昨年9月に長野県から、流通している当該製品のサンプル検査をする連絡を受け、保管ロット製品を自社で検査したところ、規格が異なることが判明した。昨年9月から納品した全国約3000医療機関から自主回収したが、回収率は16%ほどだった。多くの承認規格外製品が使用されたものと見られるが、これまでのところ、健康被害は報告されていないという。
岐阜県では昨年9月末以降、高山工場に立ち入り調査を6回実施しており、「規格外の医薬品を流通させたことによる薬事法第56条違反」として、26日以降に約10日間の高山工場の業務停止命令を行う方針。
今回の業務停止は、17日付で地元一般紙が一面で報道。社会的にも大きなインパクトを与えた。これを受け同社は17日、「今回の処分を厳粛に受けとめ深く反省し、今後かかる事故の起こらぬよう、全社を挙げて内部管理体制の強化、管理の徹底を着実に実施する所存」とし、高山工場医薬品製造業務に係る行政処分に関する謝罪文書を、医療機関などの取引先に対して発出。工場の業務停止期間も、受注業務・出荷業務は通常通り対応し、安定供給には支障を起こさないよう対応するとしている。