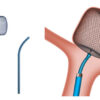
米食品医薬品局(FDA)は2020年12月23日、被包化膵壊死(walled – off pancreatic necrosis;WOPN)が生じた患者に対する、低侵襲の壊死組織除去法としてEndoRotorシステムに販売承認を与えたことを発表した。
WOPNは、重症急性膵炎(SAP)発症の数週間後に形成されることがある病変であり、致死的ともなり得る。そのため、WOPNの発生に伴い、疼痛の悪化や敗血症の原因となり得る感染症、腸閉塞などの症状が現れた際には、壊死組織の除去が必要になる。壊死組織の除去に対しては、侵襲的外科手術や、そのほかの内視鏡治療が行われているが、今回の承認により、WOPNを伴うSAP患者の15%に新たな治療選択肢がもたらされるものとFDAは推定している。
EndoRotorシステムは、パワーコンソール、フットコントロール、組織トラップ、単回使用カテーテルなどで構成される切除システムで、他の方法ではWOPNを除去できなかった場合に限り、内視鏡的壊死組織除去術(ネクロセクトミー)で使用することができる。承認は、EndoRotorシステムによる内視鏡的ネクロセクトミーを受けたWOPN患者30人を対象にした臨床試験で得られた安全性と有効性に関するデータに基づいている。EndoRotorシステムで膵臓から壊死性破片組織を除去するのに要した手順は、患者1人あたり平均2.1であった。各患者の膵臓の壊死組織の量を、処置前にCTで、処置後14〜28日目にCTや内視鏡、MRIで測定して比較したところ、処置後には壊死組織の量が平均85%、患者の半数は98.5%減少したことが明らかになった。
EndoRotorシステムに関連する重篤な有害事象が3人の患者に生じたことが報告されている(消化管出血が2人、気腹症が1人)。気腹症が生じた患者は、後に大量の感染性膵臓壊死により敗血症と多臓器不全を起こして死亡した。その他の重篤な有害事象は、吐血、深部静脈血栓症、膵炎などであり、これらは全て、デバイスではなく、患者の基礎疾患に起因して生じたものであった。
FDAは、膵臓がんが判明している患者、または膵臓がんが疑われる患者にEndoRotorシステムを用いるべきではないことを警告する枠組み警告を要求している。また、WOPN内に1 cmを超える仮性動脈瘤を伴う患者、または穿刺ルートに胃静脈瘤または回避不可能な血管が介在している患者にも禁忌である。
なお、EndoRotorシステムの販売承認は、Interscope社に対して与えられた。(HealthDay News 2020年12月29日)
Source
https://consumer.healthday.com/fda-authorizes-marketing-of-endorotor-system-2649691046.html
More Information
https://www.fda.gov/news-events/press-announcements/fda-authorizes-marketing-new-device-designed-remove-dead-pancreatic-tissue