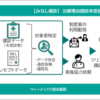
ノバルティスファーマは26日、キメラ抗原受容体T細胞(CAR-T細胞)療法「キムリア点滴静注」(一般名:チサゲンレクルユーセル)について、「再発・難治性のCD19陽性のB細胞性急性リンパ芽球性白血病(B-ALL)、再発・難治性のCD19陽性のびまん性大細胞型B細胞リンパ腫(DLBCL)」の適応で承認を取得した。CAR-T療法を採用した国内初の再生医療等製品となる。細胞採取、調製・凍結、投与後の副作用管理が行える医療機関や医師のみに限定する条件付き承認となっている。
キムリアは、患者から採取したT細胞を遺伝子導入により改変し体内に戻すことで、CD19抗原のB細胞性の腫瘍を認識して攻撃する癌免疫療法。継続的な投与を必要とせず、一度のみで治療する。米国では2017年8月に小児を含む若年成人の再発・難治性B-ALL、18年5月に成人のDLBCLに対する承認を取得している。国内の患者数は約250人を想定している。
* 全文閲覧には 薬事日報 電子版 » への申込みが必要です。