東京大学大学院薬学系研究科衛生化学教室教授 青木 淳賢

G蛋白質共役型受容体(GPCR)とその上流のリガンド産生酵素は、医薬品の主要な標的である。私が大学院の学生として研究を行っていた1990年前半までには、解熱鎮痛剤であるアスピリンは、発熱・疼痛等を引き起こすプロスタグランジン(PG)産生を担うシクロオキシダーゼの阻害すること、PGとその類縁物質であるロイコトリエン(LT)はGPCRを介し機能することなどが明らかにされていた。
様々な角度から脂質研究を行っていた井上圭三研究室に所属していた筆者は、GPCRを標的とした生理活性脂質の研究は潜在的にとても興味深いと考えていた。
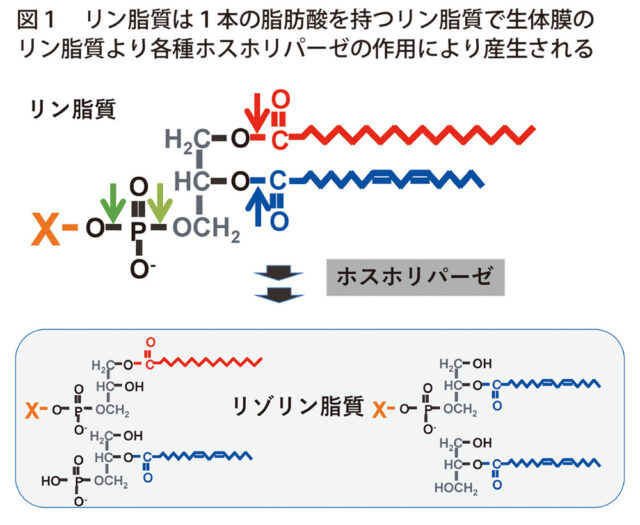
筆者は90年後半に大学助手として井上圭三研究室で研究生活をスタートしたが、その際、研究テーマとして“リゾホスファチジン酸(LPA)”に着目した。LPAはリゾリン脂質の一種であり(図1)、血圧上昇や細胞増殖効果が認められていたが、受容体、産生酵素が不明であり、個体レベルで機能を持つかについて全く不明であった。また、ラットの腹腔由来のマスト細胞がホスファチジルセリン(PS)、特に、リゾ体のPSにより効率良く脱顆粒反応を引き起こすことが知られていたため、リゾホスファチジルセリン(LysoPS)にも着目することにした。
東京大学(1996~2007、20~)と東北大学(07~20)での生理活性リゾリン脂質の研究は、多くの優秀なスタッフと学生の活躍により大きく前進した。
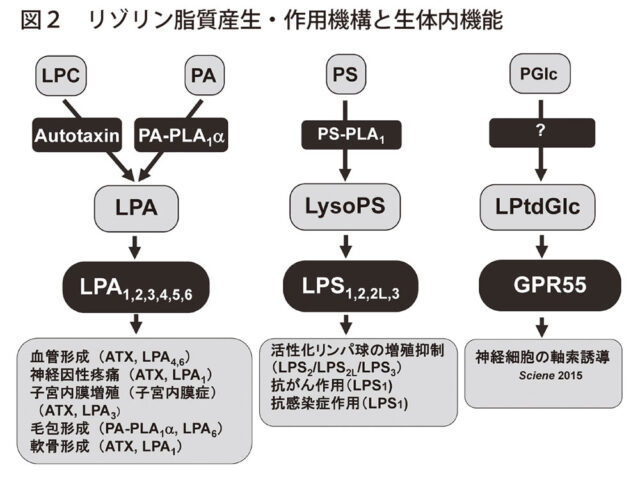
まず、LPA受容体EDG7/LPA3の同定とKOマウスを用いた生理・病態機能の解析(J Biol Cem 1999, Nature 2005, EMBO J 2017)により本受容体が受精卵着床期、受精卵を受け付けるための子宮環境を整備するために必須な働きを持つことを明らかにすることができた(図2)
また、二つのLPA産生酵素(オートタキシン[ATX]、PA-PLA1α)の同定に成功し(J Cell Biol 2002, J Biol Chem 2002)、それら産生酵素を通じLPAが血管形成、毛包形成に重要な役割を持つことを初めて明らかにすることができた(J Biol Chem 2006, EMBO J 2011)(図2)
これらの研究により、単にリン脂質の合成の中間産物、リン脂質の分解産物として考えられていたリゾリン脂質が生体内で重要な働きを持つことが明らかとなり、同時期に機能が明らかとなったLPAと類似の構造を有しGPCRを標的として機能することが判明したスフィンゴシン1リン酸(S1P)と共にリゾリン脂質メディエーターという名称で呼称されるようになった。
また、強力な免疫抑制作用を有するフィンゴリモドの作用がS1P受容体を標的としていたことや、ATXとLPAの一つの受容体であるLPA1を介するシグナルが肺線維症を誘動するシグナルであることなどが明らかとされ、リゾリン脂質メディエーターを標的とした創薬が様々な製薬企業で進められた。
現在、免疫抑制作用を有するS1P1作動薬フィンゴリモド(ジレニア)が上市され、また、LPA1拮抗薬が肺線維症の治療薬として第II相の臨床試験を通過し、第III相試験に移行している。
一方、筆者ら、特に当時、大学院生であった井上飛鳥君(現東北大薬教授)を中心に、全く新しい原理に基づくGPCR活性化測定手法“TGFα切断アッセイ”が開発された(EMBO J 2011、Nature Methods 2012)
このTGFα切断アッセイを用い、リガンドが見つかっていないオーファンGPCRのリガンドを、特に脂質に着目し実施した結果LysoPS受容体の探索もLysoPS、リゾホスファチジルグルコシド(LysoPtdGlc)、酸化リン脂質に対し応答するGPCRを複数見つけることができた。これらの新規のリゾリン脂質も、免疫調節や脳神経系において重要な生態機能を持つことも明らかにされつつある(図2)
筆者らはまた、ヒトにおけるリゾリン脂質の機能にも興味を持った。リゾリン脂質やその産生酵素が血液、脳脊髄液、精液などの体液に多く含まれることから、これら臨床サンプル中のリゾリン脂質、リゾリン脂質産生酵素を、それぞれLC-MS/MS、特異的抗体を用い検出する手法を開発した。
また、東京大学医学部附属病院検査部矢冨裕教授・部長(当時)、蔵野信教授・部長との緊密な共同研究を実施し、病態時でのリゾリン脂質、リゾリン脂質産生酵素の変動を解析した。その結果、リゾリン脂質、リゾリン脂質産生酵素は様々な病態で変動することが判明した。特に、肝硬変における血中ATX、神経障害性疼痛における脳脊髄液中のリゾホスファチジルコリン(LPC、ATXの基質)の変動が顕著であった。
ATXに関しては、東ソーと矢冨グループと全自動測定系(新規肝線維化マーカーEテスト「TOSOH」II〈オートタキシン〉)を共同開発し、これは最終的に上市されている。現在、肝線維化マーカーとして保険収載され、各病院で使用されている。
以上、筆者が30年間にわたり行ってきたリゾリン脂質に関する研究について簡単に述べさせていただいた。
リゾリン脂質の代謝・作用に関する基礎研究から始まり、KOマウスを用いる個体レベルでの機能解析、さらには、臨床レベルでの研究も実施することができたことは薬学研究者として大変幸運であったと思う。このような多角的な薬学研究が実施できたのも、多くの共同研究者に恵まれたおかげである。
また、本研究、特に基礎研究のほとんどは、東京大学大学院薬学系研究科衛生化学教室と東北大学大学院薬学研究科分子細胞生化学分野の大学院生が実施したものである。この場を借りて感謝申し上げたい。