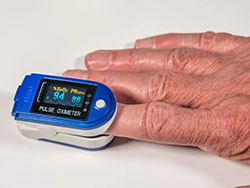
新型コロナウイルス感染症(COVID-19)パンデミックを受けて、パルスオキシメーターの使用が増加している。そんな中、米食品医薬品局(FDA)は2月19日に安全性情報(Safety Communication)を発出し、パルスオキシメーターの測定結果は、肌の色が濃い場合など特定の条件下では不正確なことがあるとして、医療従事者や患者に対して注意喚起した。
パルスオキシメーターは、指先などの皮膚に光を通して動脈血酸素飽和度(SpO2)を測定する装置である。血中酸素飽和度は一般的に96%以上が正常値とされている。FDAの今回のSafety Communicationは、「The New England Journal of Medicine」に2020年12月17日掲載された研究結果に基づいている。同研究では、パルスオキシメーターによる測定では検出されなかったにもかかわらず、血液ガス分析で潜在性低酸素血症(血液中の酸素濃度が低い)が検出される頻度が、黒人では白人の約3倍であったことが報告されている。
FDAは、「パルスオキシメーターでの測定は、血中酸素飽和度の推定に役立つが、その精度には限界とリスクのあることがエビデンスにより示されている」と指摘。その上で、患者や介護者に対しては、測定数値のみに頼るのではなく、体に生じるあらゆる兆候や症状に注意を払い、それらについて心配がある場合は医療提供者に相談することを推奨している。
一方、医療提供者に対しては、患者にパルスオキシメーターを使用する際には、血行不良や肌の色、皮膚の厚さ、皮膚温度、現在のタバコの使用状況、マニキュア使用の有無など、パルスオキシメーターの測定精度に影響を与える可能性のある要因を考慮するよう助言している。また、製品ごとに精度が異なるため、添付文書や製造元のウェブサイトを参照して、確認することを勧めている。そのほか、パルスオキシメーターの測定値は、血中酸素飽和度の推定値として使用する必要があり、診断と治療の決定は、測定値の絶対閾値ではなく、経時的な推移に基づいて行うことが望ましいとしている。
FDAは、COVID-19パンデミックの影響でパルスオキシメーターの高需要が続く見込みであることに言及し、今後もパルスオキシメーターの安全性と有効性についての評価を続けることを明言している。現状では、皮膚の色など、パルスオキシメーターでの測定結果の精度に影響を及ぼし得る要因ついて、研究データの解析を基に評価を進めている。また、市販前の製品データの追加分析や、製造業者や試験所などの外部の利害関係者との協力のもと、市販後のデータの追加分析にも取り組んでいる。
FDAは、使用しているパルスオキシメーターに関して問題があれば報告するように求めている。(HealthDay News 2021年2月23日)
More Information
https://www.fda.gov/medical-devices/safety-communications/pulse-oximeter-accuracy-and-limitations-fda-safety-communication

















